 MALATTIE A TRASMISSIONE SESSUALE (STD)
MALATTIE A TRASMISSIONE SESSUALE (STD)
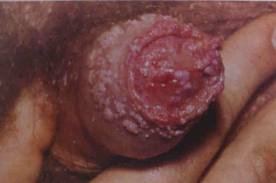
VERRUCHE GENITALI
(Condilomi acuminati; condilomi venerei)
Lesioni iperplastiche della cute o delle mucose dei genitali causate da papillomavirus umani
Eziologia
I condilomi anogenitali causati da papillomavirus umano [HPV] tipi 6, 11, 16, 18, 31, 33 e 35 sono trasmessi per via sessuale e presentano un periodo di incubazione di 1-6 mesi. Le infezioni endocervicali causate dai tipi 16 o 18 sono stati implicate nell’eziologia del tumore intraepiteliale della cervice e del cancro del collo dell’utero. I tipi 16 e 18 di HPV di solito non causano condilomi genitali esterni, che invece sono di solito causati dai tipi 6 e 11.
Sintomi e segni
Le verruche genitali si presentano come piccoli polipi rosa o grigi, molli e umidi che crescono rapidamente, possonodiventare peduncolati e spesso si ritrovano in grappoli. La superficie sembra quella di un cavolfiore. Negli uomini si manifestano nelle superfici calde e umide della regione sottoprepuziale, sul solco coronale, dentro il meato uretrale e sul corpo del pene. Nelle donne possono essere interessati vulva, parete vaginale, collo dell’utero e perineo. Sono particolarmente frequenti nella regione perianale e nel retto negli uomini omosessuali e possono essere più gravi e più diffìcili da trattare nei pazienti immunosoppressi. La velocità di crescita è variabile, ma la gravidanza, l’immunosoppressione o la macerazione della cute, possono accelerare sia la crescita sia la diffusione delle singole lesioni.
Diagnosi
Le verruche genitali possono solitamente essere identificate dal loro aspetto, ma devono essere distinte dai condilomi lati ad apice appiattito che caratterizzano la sifilide secondaria. L’effettuazione di biopsie nel caso di verruche atipiche o persistenti può rendersi necessaria onde escludere la presenza di carcinoma. Le verruche endocervicali possono essere evidenziate soltanto dalla colposcopia e non devono essere trattate fino a quando non sia disponibile il risultato di un Pap test.
Terapia
Nessuna forma di terapia risulta pienamente soddisfacente. Le recidive sono frequenti e richiedono una nuova terapia. Le verruche genitali possono essere eliminate mediante elettrocauterizzazione, laser-terapia, crioterapia o escissione chirurgica in anestesia locale o generale. Antimicotici topici quali la podofillotossina, la podofillina o il 5-fluorouracile; caustici come l’acido tricloroacetico; o induttori di interferoni, quali l’imiquimod vengono molto usati, ma solitamente richiedono applicazioni ripetute per settimane o mesi e spesso non ottengono buoni risultati. Nelle lesioni uretrali si è dimostrato efficace il tiotepa. Il 5-fluorouracile applicato localmente 2-3 volte/die dal paziente stesso, si è dimostrato efficace sulla uretra maschile, anche se sarà necessario tenere il paziente sotto controllo per l’eventuale formazione di sia pur rare ostruzioni uretrali acute. Il trattamento più soddisfacente può, tuttavia, risultare la rimozione meccanica per mezzo di un resettoscopio, in anestesia generale.
L’interferone-a, somministrato IM o direttamente nella lesione, ha eliminato lesioni intrattabili di cute e genitali. La sua modalità ottimale di somministrazione e i risultati a lungo termine non sono chiari. Un atteggiamento cauto è suggerito dai dati in merito a pazienti con papulosi bowenoide dei genitali (da virus tipo 16), nei quali le lesioni inizialmente scomparse dopo il trattamento con interferon-b si sono manifestate nuovamente in forma di cancri invasivi.
La circoncisione può prevenire eventuali recidive. I soggetti con cui il paziente avesse avuto contatti sessuali devono essere controllati e devono essere effettuati test sierologici per la sifilide inizialmente e ripetuti dopo 3 mesi. Le recidive sono frequenti e necessitano di un nuovo ciclo di trattamento.
È molto importante il follow-up delle donne con verruche genitali endocervicali e dei loro partner sessuali in modo da cogliere eventuali alterazioni displastiche o addirittura un carcinoma invasivo del collo uterino. Il riscontro di HPV tipo 16 o 18 nella papulosi bowenoide e nei carcinomi vescicali giustifca anch’esso l’effetuazione di regolari controlli a distanza. È necessario effettuare esami citologici o colposcopici sul collo uterino, da eseguirsi ogni sei mesi nel caso di donne con infezioni da tipo 16 e 18 per individuare e trattare la displasia, che talvolta è premaligna.
INFEZIONI A TRASMISSIONE SESSUALE DA CLAMIDIA, DA MICOPLASMA E DA UREAPLASMA
(Uretrite non gonococcica; uretrite non specifica; cervicite mucopurulenta; infezioni genitali aspecifiche)
Eziologia e incidenza
Sono stati identificati i microrganismi che causano la trasmissione sessuale della maggior parte dei casi di cervicite e di uretrite nelle donne, e di uretrite, proctite e faringite in ambo i sessi. Perciò i termini usati in passato per definire le forme non gonococciche di queste infezioni, ovvero uretrite non gonococcica (UNG) o uretrite non specifica, sono inesatti. Queste infezioni a trasmissione sessuale sono probabilmente le più comune STD negli USA. Gli agenti causali includono Chlamydia trachomatis (responsabile di circa il 50% dei casi di UNG e della maggior parte dei casi di cervicite mucopurulenta non gonococcica), Mycoplasma genitalium e l’Ureaplasma urealyticum; alcuni casi tuttavia risultano non spiegabili.
Sintomi e segni
Negli uomini i sintomi di uretrite compaiono abitualmente tra 7 e 28 gg dopo il contagio sessuale, con lieve disuria e fastidio uretrale con secrezione chiara o mucopurulenta. Sebbene i sintomi possano essere lievi e la secrezione moderata, essi si manifestano soprattutto al mattino quando i margini del meato possono risultare incollati da secrezioni essiccate. All’esame il meato può avere un aspetto arrossato e si possono rilevare i segni delle secrezioni sulla biancheria intima. Talvolta l’esordio è più acuto, con disuria, pollachiuria e secrezione purulenta abbondante che simula l’uretrite gonococcica. Per contatti rettali e orogenitali si possono manifestare anche proctite e faringite.
Nella maggior parte delle donne le infezioni decorrono in forma asintomatica, ma si possono riscontrare secrezione vaginale, disuria, pollachiuria, dolore pelvico, dispareunia e sintomi di faringite e di proctite. Cerviciti con essudato giallo, mucopurulento ed ectopia cervicale (espansione dell’epitelio colonnare endocervicale rosso sulla superficie vaginale della cervice) sono caratteristiche.
Diagnosi
Negli uomini gli strisci di secrezione uretrale colorati al Gram mostrano molti leucociti polimorfonucleati (PMN) e alcune cellule epiteliali, senza germi patogeni. Nei casi lievi in presenza di uretrite si procederà all’analisi delle urine, con reperto di 5 PMN/per campo (1000 ×) con lente a immersione d’olio. Se la diagnosi fosse dubbia, si eseguirà l’esame sul primo getto di urina del mattino. Se c’è infezione, un tampone uretrale raccoglie solitamente materiale sufficiente per gli esami di laboratorio che possono confermare la diagnosi. Nelle donne la colorazione di Gram su strisci di secrezioni purulente del collo uterino dimostra la presenza di molti leucociti, ma non di gonococchi.
La diagnosi dell’infezione da clamidia si basa sull’esame degli essudati infetti per evidenziare i microrganismi tramite coltura, su test immunologici per gli antigeni o su metodi genetici. Metodiche non colturali, come la colorazione con immuno fluorescenza test ELISA ed evidenziazione dell’RNA ribosomiale tramite sonde di acido nucleico, hanno reso pratica per la maggior parte dei laboratori la diagnosi di C. trachomatis dalle secrezioni genitali. Le tecniche di amplificazione degli acidi nucleici aumentano la sensibilità di rilevamento dell’RNA in modo da permetterne l’uso in entrambi i sessi. Il rilevamento del micoplasma o dell’ureaplasma è poco pratico. Lo screening per co-infezioni gonococciche è un esame di routine.
Complicanze
Negli uomini, possono verificarsi epididimiti (soprattutto in uomini < 35 aa), artrite reattiva e sindrome di Reiter (artrite con interessamento oculare e dermico e uretriti non infettive ricorrenti). Nelle donne, le complicanze includono l’artrite reattiva e la sindrome di Fitz-Hugh-Curtis, in cui l’infezione del peritoneo periepatico da Chlamydia o, meno comunemente, da gonococco può mimare la colecistite. La salpingite da clamidia di solito porta a dolore pelvico cronico, gravidanza ectopica e sterilità.
L’oftalmia neonatorum da clamidia e la polmonite possono essere causate da infezioni nei neonati partoriti da donne affette da cervicite da clamidia.
Terapia
Le infezioni non complicate vengono curate sia con la somministrazione orale di azitromicina, 1 g in unica dose, sia con ofloxacina, 300 mg bid e con tetraciclina, 500 mg q 6 h o con doxiciclina, 100 mg bid per 7 gg. I pazienti con recidive o con complicanze richiedono periodi di terapia maggiori (tetraciclina 500 mg PO q 6 h o doxiciclina 100 mg PO bid per 21-28 gg). Nelle donne in gravidanza invece della tetraciclina si somministrerà eritromicina (500 mg PO q 6 h per almeno 7 gg). Se tale posologia fosse mal tollerata, si potrà usare un dosaggio di eritromicina inferiore per un periodo di tempo più prolungato, oppure azitromicina con le posologie sopra indicate, sebbene non sia accertata la sicurezza di questo farmaco durante la gravidanza. Circa il 20% dei pazienti presenta una o più recidive nel periodo di controllo e va quindi sottoposto a un nuovo trattamento e rassicurati sul fatto che ciò porterà alla guarigione. Le infezioni da clamidia coesistono così di frequente con la gonorrea da far raccomandare la terapia presuntiva per la clamidia (v. Terapia in Gonorrea, sopra).
Se le infezioni genitali da clamidia non vengono trattate, sintomi e segni scompaiono nell’arco di 4 sett. in circa il 60-70% dei pazienti. Possono persistere infezioni cervicali croniche, che portano a endometrite cronica, salpingite o peritonite pelvica e alle conseguenze derivanti, come dolore, infertilità e gravidanze ectopiche.
Ai pazienti va consigliato di astenersi dai rapporti sessuali fino al completamento della terapia e fino a che i loro partner siano stati visitati e trattati. Dopo la cura, le persone vanno visitate di nuovo e sottoposte a test diagnostici per la ricerca di infezioni persistenti o ricorrenti, dopo 8-12 sett.
EPIDIDIMITE
L’orchi-epididimite (infiammazione dell’epididimo e del testicolo) può essere una complicanza di IVU con prostatite o uretrite, una sequela della gonorrea, una complicanza di intervento chirurgico sulla prostata o un risultato di un’infezione secondaria a un catetere a permanenza. Si presenta come una tumefazione dolorosa, dolente alla palpazione con edema scrotale ed eritema. Di solito sono coinvolti batteri gram - e Chlamydia trachomatis. L’epididimite tubercolare, la gomma luetica e le patologie micotiche (actinomicosi, blastomicosi) attualmente sono rare negli USA, con l’eccezione dei pazienti immunocompromessi (p. es., HIV).
L’epididimite batterica acuta è di solito una complicanza della batteriuria, dell’uretrite o della prostatite batterica e può essere monolaterale o bilaterale. È caratterizzata da febbre, dolore e rigonfiamento scrotale. L’esame obiettivo rivela tumefazione, indurimento, eritema e dolorabilità marcata di una porzione o di tutto l’epididimo interessato e a volte del testicolo adiacente. Quando l’infiammazione interessa il dotto deferente, ne deriva una deferentite; quando invece sono interessate anche le strutture dell’intero cordone spermatico, la diagnosi è quella di funiculite. L’organismo infettante può di solito venire identificato mediante urinocoltura. Negli uomini < 35 anni, la maggior parte dei casi è dovuta a un’infezione da patogeni trasmessi per via sessuale, soprattutto Neisseria gonorrhoeae e C. tracomatis. La maggior parte di questi uomini ha un’uretrite dimostrabile. Nella diagnosi differenziale bisogna considerare la torsione del testicolo nei pazienti di età < 30 anni. Negli uomini di età > 35 anni, la maggior parte dei casi è dovuta a batteri coliformi gram -. Questi uomini hanno piuria, urina infetta e anormalità urologiche oppure sono stati recentemente sottoposti a procedure urologiche. È indicata una valutazione genitourinaria.
L’epididimite e l’orchi-epididimite non batterica hanno un’eziologia sconosciuta ma non sono rare. Esse possono essere secondarie a spandimento retrogrado. L’esame dell’urina è spesso normale e le colture urinarie del liquido prostatico sono negative. I sintomi sono simili a quelli dell’epididimite batterica.
Terapia
Il trattamento consiste nel riposo a letto, elevazione scrotale, impacchi ghiacciati sullo scroto, analgesici e terapia antimicrobica per 7-10 giorni. Se si sospetta una sepsi, può essere utile la somministrazione parenterale di un aminoglicoside o di una cefalosporina di terza generazione, fino a che non siano noti l’organismo infettante e l’antibiogramma. Gli esami colturali sono importanti per stabilire se la terapia è adeguata. A meno di un ascesso, di un piocele o di un infarto testicolare, non è generalmente richiesto il drenaggio chirurgico. In generale, è indicata una completa valutazione urologica; tuttavia, i pazienti con epididimite trasmessa per via sessuale raramente necessitano di una valutazione anatomica.
L’epididimite batterica ricorrente, secondaria a uretrite cronica o prostatite incurabili, occasionalmente può essere prevenuta dalla legatura del deferente (vasectomia). Talvolta, l’epididimite cronica richiede un’epididimectomia per la risoluzione dei sintomi, sebbene in alcuni pazienti possa persistere un forte disagio. I pazienti che devono portare un catetere uretrale a permanenza sono predisposti a sviluppare epididimite ricorrente e orchi-epididimite. Si dovrebbe prendere in considerazione la vasectomia profilattica bilaterale nei pazienti con episodi ricorrenti per anomalie strutturali. Possono essere utili il posizionamento di una cistostomia sovrapubica o l’istituzione di un regime di autocateterizzazione.
Il trattamento dell’epididimite non batterica è simile, salvo per il fatto che la terapia antimicrobica non è efficace. Il blocco nervoso del cordone spermatico con una soluzione anestetica locale può fornire un sollievo sintomatologico.
BALANOPOSTITE
La balanopostite (infiammazione generalizzata del glande e del prepuzio) è frequentemente causata da infezioni batteriche e micotiche sotto il prepuzio del maschio non circonciso. Tale infiammazione predispone a stenosi meatale, fimosi, parafimosi e neoplasie. La balanopostite è di solito diagnosticata all’esame obiettivo da un esaminatore esperto. La malattia viene trattata con un miglioramento dell’igiene personale e, talvolta, con farmaci antimicotici. La circoncisione può essere indicata nelle complicanze o nei casi recidivanti o resistenti alla terapia.
La balanitis xerotica obliterans è un’area indurita e pallida vicino alla punta del glande, che circonda il meato e spesso provoca stenosi. È la conseguenza di un’infiammazione cronica. Si possono utilizzare farmaci antibatterici topici e antiinfiammatori. Nei casi gravi può essere indicata la meatotomia o una plastica chirurgica riparativa (meatoplastica).
L’eritroplasia di Queyrat, è un’area ben circoscritta, di pigmentazione vellutata-rossastra, che si trova di solito sul glande o sulla corona. Solitamente si verifica in uomini non circoncisi. Questa lesione precancerosa può essere istologicamente identica alla malattia di Bowen ma è in grado di diffondersi solo localmente. Si dovrebbe prendere in considerazione l’esame bioptico; la terapia consiste nell’applicazione del fluorouracile 5% in crema, nell’escissione locale o nella laser terapia. È indicato un attento follow-up.
Altre rare lesioni peniene comprendono quelle dovute a TBC, le malattie micotiche del pene e l’herpes zoster.
LINFOGRANULOMA VENEREO
(Linfopatia venerea; linfogranuloma inguinale)
Malattia sessualmente trasmessa da clamidia, caratterizzata da una lesione primaria transitoria seguita da una linfadenite suppurativa, da linfangite e da gravi complicanze locali.
Eziologia
Il linfogranuloma venereo (LGV) è provocato da diversi immunotipi di Chlamydia trachomatis differenti da quelli che provocano il tracoma, la congiuntivite da inclusi, l’uretrite e la cervicite. Questi ceppi di LGV invadono i linfonodi regionali e vi si riproducono. La malattia si riscontra soprattutto nelle zone tropicali e subtropicali e si verifica raramente negli USA.
Sintomi e segni
Dopo un periodo di incubazione da 3 a 12 gg, si forma una piccola lesione vescicolare transitoria e non indurita che si ulcera rapidamente, guarisce prontamente e può anche passare inosservata. Il primo sintomo abitualmente è l’ingrossamento unilaterale e dolente al tatto dei linfonodi inguinali, che portano poi alla formazione di una grossa massa fluttuante e dolente che aderisce ai piani profondi e infiamma la cute sovrastante. Possono svilupparsi fistole multiple che emettono materiale purulento o striato di sangue. La guarigione avviene solitamente con formazione di cicatrici, mentre le fistole possono permanere o recidivare.
Il paziente può lamentare malessere generale, febbre, cefalea, dolori articolari, anoressia e vomito. Nelle donne è frequente riscontrare mal di schiena: in esse le lesioni iniziali possono trovarsi sul collo uterino o nella porzione più alta della vagina, determinando dilatazione e suppurazione dei linfatici pelvici e perirettali. L’interessamento della parete del retto, nelle donne e negli uomini omosessuali può provocare proctite ulcerativa con secrezioni rettali purulente e striate di sangue.
Un processo infiammatorio cronico determina l’ostruzione dei vasi linfatici, portando a edema, ulcerazioni e formazione di fistole. Le grosse masse polipoidi e le ostruzioni linfatiche croniche possono determinare alla fine un’elefantiasi dei genitali. Nelle donne e nei maschi omosessuali si possono riscontrare stenosi rettali.
Diagnosi
La diagnosi clinica può essere confermata dal test di fissazione del complemento che può evidenziare un titolo anticorpale in aumento o un titolo in fase convalescente > 1:16. Un test di microimmunofluorescenza misura gli Ac tipo-specifici e distingue i vari sierotipi anticorpali. Sono disponibili in commercio kit per l’immunofluorescenza che usano anticorpi monoclonali per la colorazione di Chlamydia nel pus. Colture cellulari per Chlamydia vengono usate in un numero relativamente scarso di laboratori. In assenza di questi test la diagnosi si basa sulla tipicità del quadro clinico e su un titolo alto (> 1/ 64) o su un aumento di Ac fissanti il complemento.
Terapia
Dossiciclina, 100 mg PO bid, eritromicina 500 mg PO qid o tetracicline 500 mg PO qid, ciascun farmaco proseguito per 21 gg, consentono una rapida guarigione delle lesioni precoci. L’azitromicina probabilmente è efficace, ma non sono stati definiti il dosaggio e la durata necessari per il LGV. Il linfedema in stadio avanzato può non guarire nonostante l’eliminazione dei germi responsabili. I bubboni fluttuanti devono essere aspirati e non incisi. Ascessi e fistole richiedono l’intervento chirurgico, ma le stenosi rettali possono invece essere dilatate. L’elefantiasi si cura mediante chirurgia plastica. Tutti i soggetti che abbiano avuto rapporti sessuali con i pazienti devono essere visitati e tenuti in osservazione per 6 mesi dopo un trattamento apparentemente efficace.
GONORREA
Consiste nell’infezione dell’epitelio di uretra, cervice, retto, faringe o degli occhi causata dalla Neisseria gonorreae, che può condurre a batteriemia e può dar luogo a complicanze metastatiche.
Eziologia ed epidemiologia
L’agente causale, Neisseria gonorrhoeae, può essere messo in evidenza nelle secrezioni (mediante esame diretto del preparato tramite coltura) e ha l’aspetto di germi in coppia o a masse di diplococchi gram -, reniformi, spesso intracellulari e con le superfici di contatto appiattite o leggermente concave.
La malattia si trasmette quasi sempre per contatto sessuale. Spesso le donne sono portatrici asintomatiche dei microrganismi per settimane o mesi e spesso vengono identificati quando sono rintracciati i loro partner sessuali. Sono anche frequenti infezioni asintomatiche dell’orofaringe e del retto negli omosessuali maschi e il germe si ritrova talvolta nell’uretra di maschi eterosessuali.
La gonorrea che si presenta nella vagina o nel retto di fanciulle in età prepuberale è spesso trasmessa da adulti o per violenza sessuale o, raramente, per mezzo di oggetti contaminati.
Sintomi e segni
Negli uomini il periodo di incubazione è di 2-14 gg. L’esordio è abitualmente marcato da un lieve fastidio nell’uretra, seguito qualche ora più tardi da disuria e secrezione purulenta. Con il diffondersi dell’infezione all’uretra posteriore si manifestano poi pollachiuria e stranguria. All’esame uretrale si notano una secrezione purulenta giallo-verdastra; i margini del meato possono presentarsi arrossati ed edematosi.
Nelle donne i sintomi iniziano abitualmente dopo 7-21 gg dall’infezione. Sebbene essi siano di solito lievi, l’esordio della malattia può essere grave, con disuria, pollachiuria e secrezione vaginale. Il collo uterino e gli organi profondi dell’apparato genitale sono le sedi che più spesso vengono interessate dall’infezione, seguite dall’uretra, dal retto, dai dotti di Skene e dalle ghiandole del Bartolini. Il collo uterino può essere arrossato e di aspetto friabile, con secrezione mucopurulenta o francamente purulenta. Il pus può fuoriuscire dall’uretra per compressione sulla sinfisi pubica o può essere emesso dai dotti di Skene o dalle ghiandole di Bartolini. Una complicanza frequente è la salpingite (v. Cap. 238).
Nelle donne o negli uomini omosessuali è frequente la gonorrea rettale. Nelle donne tale manifestazione per lo più decorre in forma asintomatica, ma possono essere presenti anche fastidio perianale con secrezione rettale. Gli omosessuali maschi presentano più spesso forme di infezione rettale gravi. I pazienti possono notare le feci ricoperte di muco e pus e riferire dolore durante l’evacuazione e i rapporti anali. La faringite gonococcica derivata da contatti orogenitali è in genere asintomatica, anche se alcuni pazienti lamentano mal di gola o fastidio alla deglutizione; il faringe e la regione tonsillare possono essere arrossati e presentare essudazione talvolta con edema.
Nelle bambine e nelle fanciulle prepuberi si possono osservare irritazione, eritema ed edema della vulva con secrezione vaginale purulenta; talvolta si può associare una proctite. La fanciulla può accusare fastidi o disuria e i genitori possono notare macchie sulla biancheria intima.
Diagnosi
Uno striscio della secrezione uretrale colorato con colorazione di Gram consente una rapida identificazione del gonococco in > 90% dei soggetti di sesso maschile. Nelle donne tuttavia la colorazione di Gram su secrezioni del collo uterino è sensibile soltanto al 60%. In caso di interessamento del retto, la proctoscopia può mostrare mucopus sulle pareti del retto. In tutte le donne e negli uomini con strisci negativi o dubbi bisogna procedere all’identificazione del gonococco tramite esami colturali o metodi genetici delle secrezioni genitali. Se ci sono sintomi di infezione rettale o faringea, si raccomanda di eseguire esami colturali e metodiche genetiche in ambo i sessi, poiché la colorazione di Gram è poco sensibile e aspecifica. Le colture richiedono che gli essudati uretrali, vaginali, rettali o di altre sedi infette, siano inoculati in un terreno idoneo (p. es., terreno modificato di Thayer-Martin) e incubati a 35-36°C per 48 h in un’atmosfera contenente il 3-10% di CO2 (può essere utilizzato un contenitore a candela). Alcune colonie sono visibili dopo 24 h; la maggior parte compare dopo 48 h. Se non è possibile usufruire immediatamente di un laboratorio adatto, i campioni possono essere riposti in terreno di trasporto per essere trasferiti in laboratorio in seguito ed essere coltivati entro 48 h, preferibilmente entro 24 h.
Esami diagnostici affidabili e rapidi, basati su sonde genetiche per RNA gonococcico possono essere combinati a test per la clamidia per esaminare pazienti con uretrite o cervicite alla ricerca di entrambi i patogeni. Un test sierologico per la sifilide (TSS) va eseguito al momento della diagnosi di gonorrea e dopo 3 mesi, inoltre il paziente va sottoposto a un esame accurato in modo da escludere altre STD.
Complicanze
Negli uomini, l’uretrite postgonococcica, una complicanza ricorrente, è la conseguenza di un’infezione da altri organismi (p. es., Chlamydia trachomatis). Questi due agenti infettanti sono acquisiti contemporaneamente, ma la clamidia ha un periodo di incubazione più lungo e non risponde al trattamento con penicillina e cefalosporine. Nel quadro tipico si ripresentano in modo meno intenso secrezioni e disuria 7-14 gg circa, dopo la terapia penicillinica per la gonorrea. Le epididimiti sono rare e di solito monolaterali L’infezione risale dall’uretra posteriore lungo il dotto deferente, fino al polo inferiore dell’epididimo, che diviene dolente, caldo ed edematoso. Possono svilupparsi un idrocele secondario; ascessi delle ghiandole di Tyson e di Littré, ascessi periureterali, infezioni delle ghiandole di Cowper, della prostata e delle vescichette seminali e restringimenti uretrali sono meno frequenti. Nelle donne il problema clinico più importante è la salpingite.
L’infezione gonococcica disseminata (IGD) con batteriemia, è più comune tra le donne rispetto agli uomini. Nella sindrome dell’artrite-dermatite il paziente presenta generalmente una malattia febbrile lieve, malessere generale, poliartralgie o poliartriti migranti e con alcune lesioni cutanee pustolose, spesso alle porzioni periferiche degli arti. Ognuno di questi sintomi si presenta in circa i 2/3 dei pazienti. L’infezione genitale è spesso asintomatica, ma può essere di solito accertata con gli esami colturali. Nella metà circa dei casi è possibile isolare il microrganismo dal sangue (con maggior frequenza nella 1a sett.) o dal liquido articolare. Sono rare manifestazioni quali pericardite, endocardite, meningite e periepatite.
Anche l’artrite gonococcica, una forma più focale di IGD può essere preceduta da una batteriemia sintomatica. L’esordio è tipicamente acuto, con febbre, dolore intenso e limitazioni dei movimenti in una o in alcune articolazioni, al contrario delle IGD, in cui sono interessate più articolazioni. Le articolazioni sono gonfie e dolenti, con la cute sovrastante arrossata e calda. Il liquido sinoviale è di solito purulento (GB > 25000/ml) e contiene gonococchi che è possibile visualizzare con la colorazione di Gram oppure tramite colture. I pazienti con IGD hanno raramente colture contemporaneamente positive tanto del sangue quanto del liquido sinoviale. Dopo l’aspirazione va immediatamente instaurata la terapia onde limitare la distruzione delle superfici articolari dell’articolazione.
Possono verificarsi infezioni oculari nel neonato che possono essere prevenute con la profilassi. Si presentano raramente negli adulti
Terapia
L’emergere di gonococchi resistenti ha limitato l’utilità dei protocolli precedentemente raccomandati basati su penicillina, ampicillina e tetracicline. Le coesistenti infezioni da clamidia sono sufficientemente comuni da richiedere un trattamento presuntivo concomitante (v. oltre). Perciò si raccomanda una singola dose di ceftriaxone 125 mg IM per il gonococco più dossiciclina a 100 mg PO bid per 7 gg o azitromicina 1 g PO in unica somministrazione per la clamidia come terapia iniziale per le infezioni uretrali, endocervicali, faringee e rettali. Alternative al ceftriaxone sono una dose singola di spectinomicina 2 g IM, ciprofloxacina 500 mg PO, ofloxacina 400 mg PO, o cefixime 400 mg PO. Tutti i protocolli devono essere accompagnati da azitromicina o dalla dossiciclina per trattare le possibili coinfezioni da clamidia, con l’eccezione delle donne in gravidanza per le quali va utilizzata eritromicina 500 mg PO qid per 7 gg. Nei pazienti portatori di gonococchi di cui si conosce la sensibilità alla penicillina, si può usare amossicillina 3 g PO con probenecid 1 g PO in dose unica al posto del ceftriaxone.
Per le IGD sono considerati equivalenti ceftriaxone 1 g/die IM o EV, ceftizoxime 1 g EV q 8 h e cefotaxime 1 g EV q 8 h. Per le infezioni penicillino-sensibili, è adeguata l’ampicillina o l’amoxicillina a un dosaggio di 1 g PO q 6 h. La durata del trattamento per le IGD non è ben definita, ma i protocolli che variano da 3 a 10 gg sembrano essere ugualmente efficaci. Alcuni medici consigliano regimi terapeutici di 3 giorni con uno dei suddetti antibiotici somministrati per via parenterale insieme a un antibiotico per via orale per ulteriori 4-7 giorni.
Nell’artrite gonococcica, in cui un versamento articolare sterile può persistere per periodi prolungati può essere di beneficio l’uso di un farmaco antiinfiammatorio. Di regola non sono necessari drenaggi ripetuti, ma all’inizio si può tenere l’articolazione immobilizzata in una posizione funzionale. Si dovranno avviare al più presto possibile esercizi di mobilizzazione passiva e, se è interessato il ginocchio, gli esercizi di rafforzamento del quadricipite. Quando scompare il dolore, si eseguiranno esercizi più attivi almeno due volte/die, con stiramento, escursioni attive e rinforzo muscolare. Oltre il 95% dei pazienti affetti da artrite gonococcica, trattato adeguatamente, può recuperare la funzione articolare in modo completo.
La possibilità di trasmissione della gonorrea va spiegata al paziente, il quale deve astenersi dall’attività sessuale sino a quando sia la terapia per la gonorrea sia quella per la clamidia non sia completata. È necessario individuare, esaminare e trattare i partner sessuali dei pazienti.
Non è necessario sottoporre a test il paziente subito dopo il trattamento anti-gonococcico per confermare che il paziente non sia più contagioso sempre che la risposta sintomatica sia stata adeguata. La ripetizione dello screening per un’eventuale reinfezione da clamidia o da gonococco è consigliata dopo 4-8 sett. Un TSS va effettuato sebbene la maggior parte delle infezioni sifilitiche concomitanti è curata dai farmaci utilizzati per il trattamento della gonorrea.
SIFILIDE
Malattia contagiosa sistemica provocata dalla spirocheta Treponema pallidum e caratterizzata da stadi clinici sequenziali e da anni di latenza.
La sifilide acquisita o congenita può interessare più organi od organi isolati, tanto da farle avere una cattiva reputazione per la sua capacità di essere scambiata per altre malattie.
SIFILIDE ACQUISITA
Eziologia e anatomia patologica
Il T. pallidum è un fragile organismo a spirale di circa 0,25 mm di larghezza e da 5 a 20 mm di lunghezza, che viene riconosciuto per la caratteristica morfologia e per la sua mobilità con un microscopio in campo oscuro o con tecniche fluorescenti (v. in Diagnosi, oltre). Esso non cresce nei normali terreni di coltura, si riproduce scarsamente nelle colture di tissutali e non può sopravvivere a lungo fuori del corpo umano.
Nella sifilide acquisita il T. pallidum penetra nell’organismo attraverso le membrane mucose o la cute, raggiunge i linfonodi periferici nel giro di poche ore e rapidamente si dissemina in tutto l’organismo. Durante tutti gli stadi della malattia l’infiltrazione perivascolare di linfociti, plasmacellule e in seguito di fibroblasti causa edema e proliferazione endoteliale dei piccoli vasi sanguigni fino a causare un’endoarterite obliterante. Nella sifilide tardiva, il T. pallidum porta alla formazione di masse simil granulomatose (gomme) che causano reazione, ulcerazioni e necrosi. Il processo infiammatorio può ridursi malgrado il danneggiamento progressivo, in particolare a carico del sistema cardiovascolare e del sistema nervoso centrale.
Il SNC viene invaso nelle fasi precoci dell’infezione. Nella fase secondaria della malattia > 30% dei pazienti presenta un LCR con caratteristiche anormali e può presentare sintomi di meningite.Durante i primi 5-10 anni dall’infezione la malattia interessa soprattutto le meningi e i vasi sanguigni, provocando la neurosifilide meningovascolare. Più tardi risultano danneggiati il parenchima cerebrale e il midollo spinale, con lo sviluppo di neurosifilide parenchimatosa. L’interessamento della corteccia cerebrale e delle meningi che la ricoprono porta alla paresi generale. La distruzione delle colonne posteriori e dei gangli dorsali del midollo spinale produce la tabe dorsale.
Epidemiologia
Tra la fine degli anni ’80 e l’inizio dei ’90, l’incidenza della sifilide primaria e secondaria è raddoppiata nei neri (in concomitanza all’uso di cocaina e alla diffusione della prostituzione), ma l’incidenza è diminuita in tutti i gruppi etnici verso la metà degli anni ’90. Questo miglioramento viene attribuito alle aggressive misure di sanità pubblica (quali l’identificazione dei contatti sessuali).
L’infezione si trasmette solitamente per contatto sessuale, compresi i contatti orogenitali e anorettali e talvolta anche attraverso il bacio e i contatti corporei intimi. Le lesioni cutanee nella sifilide primaria, secondaria, o latente precoce, sono responsabili della trasmissione praticamente in tutti i casi, tranne nella malattia congenita. La sifilide latente tardiva o la terziaria non sono contagiose. L’infezione trattata non conferisce immunità nei confronti di successive reinfezioni.
Sintomi, segni e decorso
Il periodo d’incubazione della sifilide primaria varia da 1 a 13 sett., ma abitualmente è di 3-4 sett. La malattia si può presentare in qualsiasi stadio e anche a grande distanza di tempo dall’infezione iniziale. Poiché la malattia presenta manifestazioni cliniche molteplici ed è attualmente rara nella maggior parte dei paesi industrializzati, è possibile che i medici trovino in pratica qualche difficoltà nel riconoscerla. Il decorso clinico della sifilide può essere accelerato da una coesistente infezione da HIV. In questi casi possono essere più frequenti l’interessamento oculare e la meningite.
Sifilide primaria: la lesione primaria o sifiloma in genere evolve e si rimargina entro 4-8 sett. nei pazienti non trattati. Dopo l’infezione, una papula rossa si sgretola in poco tempo dando luogo a un’ulcera indolore a base indurata che, quando viene abrasa, emette una secrezione sierosa limpida che contiene numerose spirochete. I linfonodi regionali sono di solito ingrossati e non dolenti e appaiono sodi, separati e non sensibili alla pressione. I sifilomi compaiono sul pene, nell’ano e nel retto nei maschi; sulla vulva, sul collo uterino e sul perineo nelle femmine. I sifilomi possono anche comparire sulle labbra o sulle membrane mucose dell’orofaringe o nelle regioni anogenitali. Raramente si possono riscontrare sulle mani o in altre parti del corpo, ove spesso provocano sintomi tanto lievi da passare inosservate.
Sifilide secondaria: le eruzioni cutanee compaiono solitamente tra 6 e 12 sett. dopo l’infezione e raggiungono la fase più florida dopo 3-4 mesi. Circa il 25% dei pazienti presenta sifilomi primari residui. Le lesioni possono essere transitorie o possono persistere per mesi. Se non vengono trattate esse per lo più guariscono, ma possono apparirne di nuove nell’arco di settimane o di mesi. Di frequente, si apprezzano una moderata linfadenopatia generalizzata, con linfonodi duro-elastici, non molli ed epatosplenomegalia. Oltre l’80% dei soggetti presenta lesioni mucocutanee; il 50% presenta un ingrossamento generalizzato dei linfonodi e circa il 10% ha lesioni oculari (uveite), ossee (periostite), articolari, meninge, renali (glomerulite), epatiche e spleniche. Sono spesso presenti lievi sintomi costituzionali come febbre, malessere generale, cefalea, anoressia, nausea, dolori alle ossa e affaticabilità, insieme a sintomi come anemia, ittero e albuminuria. Si può sviluppare una meningite sifilitica acuta, con cefalea, rigidità cervicale, lesioni dei nervi cranici, sordità e talvolta edema papillare.
Le eruzioni cutanee della sifilide possono simulare un’ampia gamma di patologie dermatologiche (v. oltre in Diagnosi). Esse sono spesso simmetriche e più marcate sulle superfici flessorie e volari del corpo, in particolare alle palme delle mani e alle piante dei piedi. Le eruzioni si presentano spesso a grappoli e possono essere costituite da macule, papule, pustole o lesioni squamose. Le singole macchie sono pigmentate nei neri e di colore rosaceo o rosso chiaro nei bianchi; sono rotonde e tendono a divenire confluenti e indurite, ma non danno prurito. Alla fine vanno incontro a guarigione senza lasciare cicatrici, ma talvolta residuano aree di iperpigmentazione o di depigmentazione.
Le membrane mucose spesso si erodono, formando chiazze mucose circolari e sovente bianco-grigiastre con un’areola rossa. Queste chiazze si presentano soprattutto nella bocca, su palato, faringe, laringe, su glande, pene e vulva, canale anale e retto. I condilomi lati sono delle papule ipertrofiche, piatte, rosa spento o grigio presenti alle giunzioni mucocutanee e nelle aree umide della cute e sono oltremodo contagiose. I peli spesso cadono a chiazze e determinano un aspetto come di “stoffa tarmata” (alopecia areata).
Stadio latente: questo stadio può risolversi spontaneamente in pochi anni o può durare per l’intera vita del soggetto. Nel periodo latente precoce (< 2 anni dopo l’infezione) possono verificarsi le recidive mucocutanee infettive, ma dopo 2 anni tale evento è raro e il paziente appare normale. Circa 1/3 delle persone non trattate sviluppa la sifilide tardiva anche se non prima di diversi anni dall’infezione iniziale. Nei pazienti che hanno ricevuto terapie antibiotiche per altre patologie, la sifilide terziaria può guarire, evenienza questa che può spiegare la rarità della sifilide terziaria nei paesi industrializzati.
Sifilide tardiva o terziaria: le lesioni si possono clinicamente distinguere in: (1) sifilide terziaria benigna di cute, ossa e visceri; (2) sifilide cardiovascolare; (3) neurosifilide.
Sifilide terziaria benigna: le lesioni si sviluppano abitualmente entro 3-10 anni dall’infezione, ma sono praticamente scomparse dopo l’avvento degli antibiotici. La lesione tipica è rappresentata dalla gomma luetica, una massa infiammatoria che evolve nella necrosi e nella fibrosi, spesso localizzata, ma talvolta diffusamente infiltrante organi e tessuti. Le lesioni localizzate sono formate da un’area di necrosi centrale circondata da tessuto di granulazione. Le gomme non danno dolore, crescono lentamente, guariscono con gradualità e lasciano cicatrici. Esse possono svilupparsi sulla cute, dove producono eruzioni nodulari, ulcerative o squamose. Nel sottocutaneo, esse provocano ulcere a stampo con sfaldamento necrotico e basi dall’aspetto di cuoio lavato. Le ulcere una volta guarite lasciano cicatrici atrofiche (a carta igienica). Le gomme spesso si verificano nei tessuti sottomucosi (specialmente su palato, setto nasale, faringe e laringe) e portano a perforazione del palato o del setto nasale. Anche se sono più frequenti sulle gambe, nella porzione superiore del tronco, sul volto e sul cuoio capelluto, possono svilupparsi praticamente in qualsiasi zona del corpo.
La sifilide terziaria benigna delle ossa produce o una periostite con neoformazione ossea o un’osteite con lesioni erosive che causano un dolore sordo e incessante che peggiora durante la notte. È possibile palpare un rigonfiamento o una protuberanza.
Sifilide cardiovascolare: sono presenti un aneurisma toracico, di solito filiforme dell’aorta ascendente o trasversa, restringimento degli ostii coronarici o insufficienza delle valvole aortiche che compaiono abitualmente da 10 a 25 anni dopo l’infezione iniziale.
Neurosifilide: una forma asintomatica di neurosifilide precede in genere la neurosiflide sintomatica e si riscontra nel 15% circa dei soggetti cui in origine era stata diagnosticata una sifilide latente, nel 12% dei soggetti con sifilide cardiovascolare e nel 5% dei soggetti con sifilide terziaria benigna. Possono esserci alterazioni del LCR (v. oltre in Diagnosi). La neurosifilide sintomatica produce varie sindromi cliniche nel 5% circa delle infezioni non trattate.
Nella neurosifilide meningovascolare l’interessamento cerebrale si manifesta con cefalea, vertigini, scarsa capacità di concentrazione, stanchezza, insonnia, rigidità del collo e visione offuscata. Possono manifestarsi anche confusione mentale, attacchi epilettiformi, edema della papilla, afasia e mono-o emi-plegia. Paralisi dei nervi cranici e anomalie della pupilla di solito indicano una meningite basilare. La pupilla di Argyll Robertson, che si osserva quasi esclusivamente nella neurosifilide, è una pupilla piccola e irregolare che accomoda normalmente con la convergenza, ma non reagisce alla luce.
L’interessamento del midollo spinale può produrre sintomi bulbari, debolezza e deperimento dei muscoli del cinto scapolare e delle braccia, paraplegia spastica a lenta progressione con sintomi vescicali e, in rari casi, mielite trasversa con paraplegia flaccida improvvisa e perdita del controllo degli sfinteri.
Neurosifilide parenchimatosa (una paresi generalizzata o demenza paralitica) colpisce in genere pazienti di 40-50 anni e si manifesta con deterioramento comportamentale progressivo e può simulare una malattia psichiatrica o il morbo di Alzheimer. Possono essere presenti convulsioni, afasia o emiparesi transitorie, ma sono più comuni irritabilità, difficoltà di concentrazione, deterioramento della memoria, errori di valutazione, cefalee, insonnia o spossatezza. L’igiene e l’aspetto generale del soggetto si deteriorano. Possono anche verificarsi instabilità emotiva, astenia, depressione e manie di grandezza con perdita dell’introspezione.
I segni fisici comprendono tremori della bocca, della lingua, mani iperestese, tremori in tutto il corpo; anomalie pupillari, disartria, riflessi tendinei vivaci e, in alcuni casi, risposte plantari estensorie. La calligrafia è spesso tremula e illegibile. Le lesioni delle colonne posteriori della tabe dorsale (atassia locomotoria) provocano dolore, atassia, alterazioni della sensibilità e perdita dei riflessi tendinei. Il sintomo più precoce e più caratteristico è abitualmente un dolore intenso e lancinante (dolore fulminante) alla schiena e alle gambe che si presenta con recidive irregolari. Andatura atassica, iperestesia e parestesia possono accompagnarsi alla sensazione di camminare su gomma piuma. La perdita della sensibilità vescicale può determinare ritenzione urinaria, incontinenza e infezioni ricorrenti. Un reperto frequente è l’impotenza.
La maggior parte dei pazienti con tabe dorsale è magra e ha una caratteristico facies triste e le pupille di Argyll Robertson. Può presentarsi atrofia del nervo ottico. L’esame delle gambe rivela ipotonia, riflessi tendinei ridotti o assenti, ridotta sensibilità alle vibrazioni e alla posizione delle articolazioni, atassia nel test calcagno-tibia e assenza delle sensazioni dolorifiche profonde e segno di Romberg.
Altre lesioni: le crisi viscerali si manifestano sotto forma di dolori parossistici a livello di vari organi, le più frequenti sono quelle gastriche con vomito. Si riscontrano anche crisi rettali, vescicali e laringee. Nelle fasi successive della malattia possono manifestarsi lesioni trofiche, secondarie a ipoestesia della cute o dei tessuti periarticolari. Sulla pianta dei piedi si possono sviluppare ulcere trofiche, che penetrano in profondità e interessano le ossa sottostanti. È comune l’artropatia di Charcot, disordine indolore delle articolazioni, con rigonfiamento osseo ed escursione di movimento anomala.
Diagnosi
Gli studi diagnostici per la sifilide includono un’anamnesi clinica orientata, un esame fisico, test sierologici, indagini sui contatti sessuali e nel caso un esame microscopico in campo oscuro dei liquidi emessi dalle lesioni, test sul LCR ed esami radiologici.
Sono due le classi di test sierologici per la sifilide (TSS) che aiutano nella diagnosi della sifilide e delle altre malattie da treponemi: i test di screening che utilizzano antigeni lipoidei non treponemici evidenziano le reagine sifilitiche e includono il Venereal Disease Research Laboratory (VDRL) e la reagina plasmatica rapida (RPR). I test treponemici specifici evidenziano gli anticorpi antitreponemici e comprendono il test di assorbimento di Ac anti-treponema fluorescenti (FTA-ABS), il saggio di microemoagglutinazione per gli Ac contro T. Pallidum (MHA-TP) e il test di emoagglutinazione per il Treponema pallidum (TPHA).
Il test VDRL è un saggio di flocculazione per la sifilide in cui l’anticorpo reaginico (da non confondere con gli Ac detti reagine che sono mediatori dell’allergia) nel siero del paziente si lega con evidenza con la cardiolipina, l’Ag. In numerose malattie (p. es., in corso di epatite acuta) si può avere un aumento di Ac reaginici e una positivizzazione del test VDRL. Il risultato di tale test è formulato come: reattivo, debolmente reattivo, limite (borderline) o non reattivo. I sieri reattivi e debolmente reattivi sono considerati positivi per gli Ac anti-sifilide. Tutti i test VDRL con un simile risultato positivo (reattivo o debolmente reattivo) vanno confermati con uno o più test treponemici maggiormente specifici e i test reattivi vanno quantizzati tramite diluizioni seriate.
I test di screening sono semplici da eseguire e poco costosi, ma non possiedono la specificità dei test treponemici e danno talvolta risultati falsamente positivi (FP). Un risultato FP (definito come un test reaginico reattivo, ma con test treponemico non-reattivo) può indicare una malattia vascolare autoimmunitaria, una collagenopatia, infezioni virali o condizioni caratterizzate da immunoglobuline alterate.
I titoli reaginici quantitativi diminuiscono dopo la terapia, diventando negativi nell’arco di 1 anno nella sifilide primaria e di 2 anni nei casi secondari. I test reaginici non diventano positivi prima di 3-6 sett. dall’infezione iniziale. Poiché il sifiloma primario si manifesta prima di tale epoca, un TSS precoce negativo non può escludere la sifilide. Nei pazienti con lesioni genitali non diagnosticate, i test reaginici devono dare risultati non reattivi alla sesta sett. prima che si possa escludere la diagnosi di sifilide. I test treponemici solitamente divengono positivi entro 3-4 sett. e restano tali per molti anni, nonostante il paziente abbia effettuato una terapia efficace.
Nella microscopia in campo scuro la luce viene diretta obliquamente attraverso il vetrino in modo che i raggi di luce che colpiscono le spirochete le fanno apparire luminose, mobili, attorcigliate, su sfondo scuro. Il microrganismo deve essere distinto morfologicamente da altre spirochete non patogene, che possono fare parte della normale flora, specialmente di quell’orale. Prima di procedere alla terapia, al fine di escludere la neurosifilide, viene raccomandato lo svolgimento dell’esame del LCR (eccetto in presenza di infezioni sviluppatesi da meno di 1 anno). Si effettuano d’abitudine la conta delle cellule, la conta differenziale, il dosaggio delle proteine totali, il test VDRL o altri test sierologici aspecifici (reaginici). I test treponemici sul LCR non sono utili.
Sifilide primaria: la diagnosi dipende dalla dimostrazione della presenza di T. Pallidum negli essudati prelevati dal sifiloma primario, come si può rilevare con l’esame microscopico in campo scuro. Se questa prova fosse negativa, essa andrà ripetuta e completata con i TTS. Gli ago aspirati da linfonodi possono mettere in evidenza il T. pallidum in quei casi in cui sia manifesta un’adenopatia.
La diagnosi differenziale delle ulcere genitali comprende herpes genitalis, cancroide, linfogranuloma venereo, scabbia escoriata, chiazze mucose della sifilide secondaria, balanite erosiva, malattia di Behçet, ulcere gommose, epitelioma, granuloma inguinale e traumi. Le coinfezioni sostenute da due patogeni (p. es., herpes simplex e treponema), non sono rare. (Nota: tutte le ulcere genitali devono essere considerate sifilitiche fino a prova contraria.) I sifilomi extragenitali spesso non vengono diagnosticati correttamente perché non si prende in considerazione la possibilità che si tratti di sifilide.
Sifilide secondaria: poiché la sifilide può somigliare a molte malattie della cute, è necessario prevedere la possibilità che una qualsiasi eruzione cutanea o mucosa non ancora diagnosticata possa essere dovuta alla sifilide, specialmente se si associa a una linfoadenopatia generalizzata o se si presenta in pazienti a rischio per questa malattia. La diagnosi si precisa con la dimostrazione della presenza del T. pallidum nei preparati microscopici in campo oscuro oppure esclusa da un TTS negativo, che è viceversa sempre positivo a questo stadio, spesso con un alto titolo di anticorpi anti-reagine. Un TTS positivo non permette di concludere che una malattia cutanea sia di natura sifilitica, in quanto una sifilide latente può coesistere con altre patologie cutanee. La sifilide secondaria può essere confusa con eruzioni da farmaci, pityriasis rosea, rosolia, mononucleosi infettiva, eritema multiforme, pityriasis rubra pilaris o con infezioni da funghi. I condilomi lati possono essere scambiati per verruche, emorroidi o pemfigo vegetante; le lesioni del cuoio capelluto possono essere scambiate per scabbia o alopecia aerata idiopatica, mentre le chiazze mucose per varie altre affezioni.
Stadio latente: la diagnosi, nei pazienti con TSS reaginici e treponemici ripetutamente positivi e senza lesioni sifilitiche attive, si pone per esclusione rispetto ad altre forme di sifilide. Il LCR risulta normale, così pure il cuore e l’aorta agli esami clinici e radiologici. La sifilide latente acquisita deve essere distinta dalla sifilide latente congenita, dalla framboesia latente, da altre malattie treponemiche e dalle reazioni FPB. Dal momento che molti pazienti non hanno una storia di manifestazioni primarie o secondarie, si deve supporre che essi siano stati asintomatici nelle fasi precoci, che abbiano avuto manifestazioni trascurabili o che la diagnosi sia stata omessa.
Sifilide terziaria: nella sifilide terziaria benigna i TSS sono positivi nella maggior parte dei casi, ma senza la biopsia sarà difficile distinguere questa condizione da altre masse infiammatorie o da ulcere. Nella sifilide cardiovascolare i sintomi e i segni sono talvolta così tipici da consentire una diagnosi presuntiva solo su base clinica. Sono reperti indicativi di aortite sifilitica l’ingrandimento dell’arco aortico e le calcificazioni lineari sulle pareti dell’aorta ascendente all’esame radiologico del torace; il reperto all’esame obiettivo di un suono alto, musicale del secondo tono aortico; insufficienza cardiaca; il dolore toracico e la dispnea parossistica notturna. Può essere presente un’insufficenza aortica sifilitica, senza una stenosi aortica importante. Gli aneurismi sifilitici possono provocare sintomi da compressione o da erosione delle strutture adiacenti nel mediastino e nella parete toracica, fra cui tosse profonda e respiro stridulo da compressione sulla trachea, stenosi bronchiale e successivamente infezione secondaria a compressione sull’esofago, raucedine, come conseguenza della compressione del nervo laringeo ricorrente ed erosione dolorosa dello sterno e delle costole o della colonna vertebrale per le ripetute pulsazioni dell’aorta dilatata.
La diagnosi può essere confermata mediante esami ecocardiografici, radiologici, ECG e TSS. Si dovrà esaminare anche il LCR, perché sifilide cardiovascolare e neurosifilide possono presentarsi contemporaneamente. Nella neurosifilide asintomatica il LCR presenta solitamente una conta cellulare elevata, un’aumentata proteinorrachia e test reaginici positivi. Nelle paresi i test treponemici nel siero sono positivi e il LCR risulta sempre anormale, con conte leucocitarie di 7-100 linfociti/ml, proteinorrachia aumentata e test reaginici positivi. Nella tabe dorsale i test treponemici sierici sono solitamente positivi, ma i test reaginici di screening possono risultare negativi. Il LCR presenta abitualmente una conta cellulare elevata, livelli proteinici elevati e TSS debolmente positivi. In molti casi avanzati il LCR può essere normale.
Terapia
La penicillina è l’antibiotico di scelta per qualsiasi stadio della sifilide. Per curare la sifilide infettiva precoce è necessario un livello sierico di 0,03 UI/ml per 6-8 gg. La benzatin penicillina G, 2,4 milioni U IM in unica dose, produce livelli ematici soddisfacenti per circa 2 sett. (solitamente si iniettano 1,2 milioni U in ciascuna natica). Nella sifilide secondaria e latente si praticano altre due iniezioni di 2,4 milioni di U q 7 gg, a causa della persistenza occasionale dei treponemi nel LCR dopo i protocolli monodose. In alternativa, si può somministrare penicillina G procaina, 600000 U/die IM per 10 gg, che però non presenta vantaggi particolari. Per i pazienti allergici alla penicillina, si può utilizzare ceftriaxone 1 g IM q 3 gg diluito in 3,6 ml di lidocaina all’1% per 4 somministrazioni, eritromicina oppure tetraciclina, 500 mg PO q 6 h per 15 gg o doxiciclina 100 mg PO bid per 14 giorni, ma l’efficacia di questi farmaci non è ben definita. Gli ultimi tre regimi terapeutici vanno controllati con attenzione, perché è necessaria un’attiva partecipazione dei pazienti.
Sifilide primaria e secondaria: bisogna spiegare al paziente tutte le particolarità del caso. Bisogna rintracciare tutti gli individui con cui il soggetto abbia avuto contatti sessuali negli ultimi 3 mesi (per i casi di sifilide primaria) o nell’ultimo anno (per i casi di sifilide secondaria): tali individui andranno esaminati, curati e informati del fatto che essi possono essere portatori dell’infezione e contagiosi. Essi devono evitare i rapporti sessuali finché, insieme ai rispettivi partner, non siano stati esaminati e non abbiano completato la terapia.
Sifilide latente precoce e tardiva: i pazienti devono essere trattati con penicillina, come descritto sopra, allo scopo di impedire lo sviluppo successivo delle manifestazioni terziarie. I pazienti intolleranti alla penicillina possono essere trattati con uno qualunque dei regimi alternativi sopra indicati, ma si sa ancora meno sulla loro efficacia di quanto non si sappia in caso di sifilide primaria.
Sifilide terziaria: la sifilide terziaria benigna si tratta allo stesso modo della sifilide latente; nei soggetti che non tollerano la penicillina e che vengono curati con eritromicina, si consiglia di effettuare un secondo ciclo terapeutico a distanza di 3 mesi.
Dal momento che i pazienti con sifilide in stadio successivo a quello primario e con una concomitante infezione da HIV, hanno tassi di complicanze aumentati, essi devono essere regolarmente sottoposti a esame per rinvenire tracce di neurosifilide e sifilide oculare e i protocolli di trattamento devono essere programmati a seconda dei casi.
La terapia per la sifilide cardiovascolare è la stessa della sifilide latente, ma di solito si somministra la penicillina G procaina per un totale di 21 gg.
Per la neurosifilide si usa la penicillina acquosa, 2 g EV q 4 h per 10 gg, poiché penetra al meglio il LCR, anche se il farmaco è di uso poco pratico. La procaina penicillina G 600000 U più 1 g di probenecid o ceftriaxone 1 g IM o EV die per 14 giorni, oppure amoxicillina, 3 g PO bid, associata a probenecid, si sono dimostrati efficaci. La terapia della neurosifilide asintomatica previene lo sviluppo della neurosifilide sintomatica, ma abitualmente non determina la regressione dei sintomi già comparsi. Il trattamento della sifilide oculare o della neurosifilide nelle persone con infezione da HIV può essere più difficile.
La paresi si può controllare con successo mediante antipsicotici somministrati oralmente o IM. Nei soggetti tabetici con dolori intensi si possono usare liberamente antidolorifici; p. es., può risultare utile la carbamazepina 200 mg PO tid o qid.
Oltre il 50% dei pazienti con sifilide precoce infettiva e in particolare quelli con sifilide secondaria presenta una reazione di Jarisch-Herxheimer entro 6-12 h dall’inizio della terapia. La reazione, che si manifesta con malessere generale, febbre, cefalea, sudorazione profusa, brividi o temporanea riesacerbazione delle lesioni sifilitiche, scompare abitualmente nel giro di 24 h e non presenta alcun pericolo se non lo stato d’ansia che essa può provocare. Tuttavia i pazienti con paresi generalizzata o con conte cellulari elevate nel LCR possono sviluppare una reazione di Jarisch-Herxheimer che talvolta provoca conseguenze gravi, come attacchi epilettici o infarti. Bisogna spiegare al paziente la natura della reazione prima di iniziare il trattamento. Le reazioni di Jarisch-Herxheimer possono essere confuse con l’allergia agli antibiotici e possono rappresentare un indizio della presenza di sifilide in soggetti sottoposti a terapia per altre cause, con antibiotici attivi nei confronti dei treponemi.
Sorveglianza post-terapia
L’importanza della ripetizione dei test per confermare l’avvenuta guarigione va illustrata al paziente prima dell’inizio della terapia. Si dovranno eseguire gli esami e i test reaginici quantitativi a 1, 3, 6 e 12 mesi oppure, dopo il dodicesimo mese, finché il risultato non sia negativo. Dopo il successo terapeutico le lesioni guariscono rapidamente, i titoli sierologici cadono e i test reaginici diventano abitualmente negativi nel giro di 9-12 mesi. I test treponemici, come l’FTA-ABS e il MHA-TP invece restano positivi per anni o per sempre. Il LCR va controllato dopo 1 anno di sorveglianza. Se il test VDRL resta positivo per > 1 anno o se il titolo incomincia a salire, bisognerà prendere in considerazione la ripetizione del ciclo terapeutico. Le recidive sierologiche o cliniche sono rare, ma talvolta si verificano tra il 6o e 9o mese e in particolare a carico del sistema nervoso. Le recidive richiedono la ripresa della terapia con dosaggi superiori di antibiotici, ma andrà anche presa in considerazione la possibilità di una reinfezione. Se tutti gli esami clinici e sierologici restano a livelli soddisfacenti per 2 anni dopo la terapia, si potrà informare il paziente del raggiungimento della guarigione.
Tutti i pazienti affetti da sifilide devono essere incoraggiati a sottoporsi al test per il HIV. Le persone affette da sifilide primaria o secondaria che risultano sieronegative, devono essere sottoposte nuovamente al test HIV dopo 6 mesi.
I pazienti con sifilide latente vanno controllati ed esaminati dopo 3, 6, 12, 18 e 24 mesi. I soggetti con TTS ripetutamente positivi vanno sottoposti a controlli annuali per tutta la vita. La prognosi è eccellente. I pazienti con sifilide terziaria benigna vanno controllati a intervalli regolari dopo la terapia e quelli con sifilide cardiovascolare devono essere seguiti per tutta la vita. I pazienti con aortite sifilitica non complicata possono avere una sopravvivenza normale e un decorso prolungato, ma gli aneurismi aortici sifilitici hanno una prognosi infausta. La durata media della vita dopo l’insorgenza dei sintomi è di circa 6 mesi. Nella neurosifilide asintomatica, il LCR deve essere esaminato q 6 mesi oppure fino a 2 anni dopo il ritorno alla normalità. Se il LCR è anormale, esso va esaminato q 3 mesi fino a normalizzazione dei parametri e quindi annualmente per altri 2 anni. La tabe dorsale tende a progredire malgrado la terapia.
